シグマトロピー転位は、二重結合や三重結合、あるいは芳香環など、π電子を含む多重結合官能基と隣接する単結合が電子の流れによって切れたり繋がったりする反応です。
シグマトロピー転位だけで長編ブログが書けてしまいそうなので、またそのうち取り上げたいと思いますが、個人的なイメージでは電子がくるくる回って最終的により安定なものに落ち着く、とでも言いましょうか。
まぁ、もう少しちゃんと勉強してからにしますね。
今日は、最もよく知られている[3,3]-シグマトロピー転位のうち、Johnson-Claisen rearrangement(ジョンソン-クライゼン転位)について考えたいと思います。
アリルアルコールがオルト酢酸エステルによって2炭素伸長するジョンソン-クライゼン転位
[3,3]-シグマトロピー転位の中でも、Cope転位とClaisen転位はたびたび有機合成に利用されています。
Cope転位では反応に関わる6個の原子がすべて炭素ですが、Claisen転位では酸素原子を1つ含んでいるのが特徴ですね。
オリジナルのClaisen転位も有用性が高い反応ですが、より使いやすいように多くの改良法が知られていて、ジョンソン-クライゼン転位もそのうちのひとつです。
アリルアルコールに対してオルト酢酸エステルを酸触媒とともに加熱すると、原料の炭素-炭素二重結合のうち、アルコールから遠いほうの炭素に2炭素伸びたエステルが形成されます。
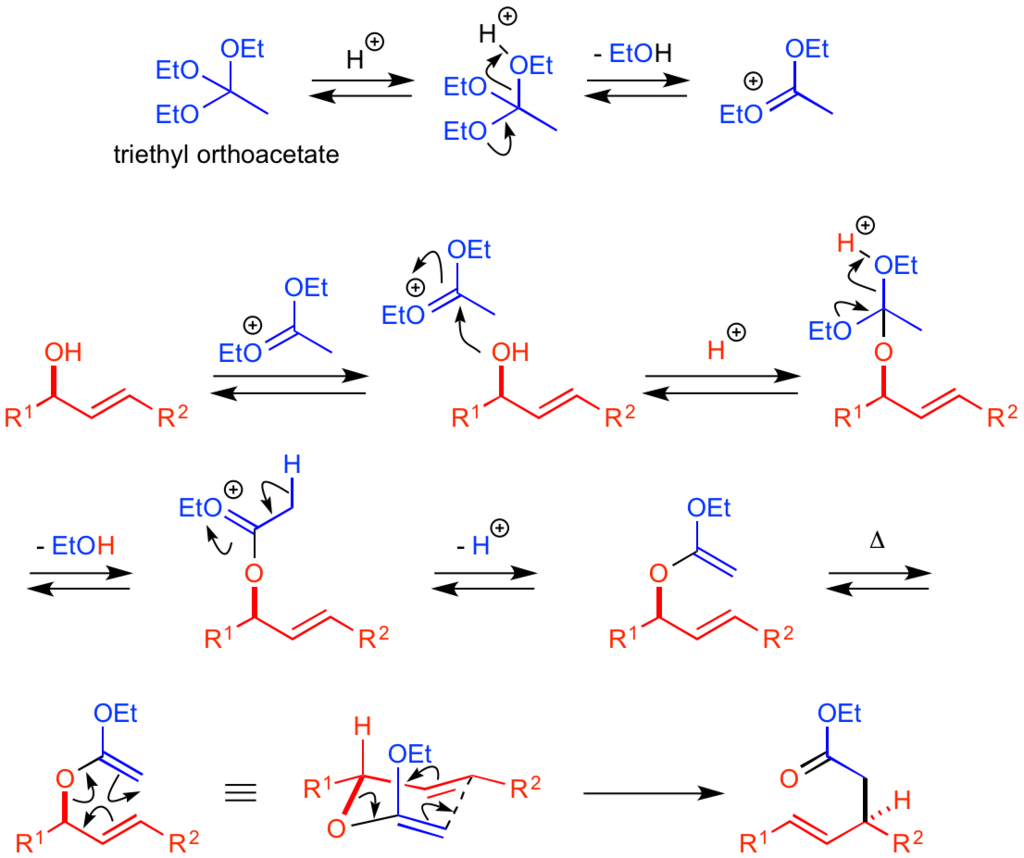
Johnson-Claisen転位の反応機構では、まず酸触媒によって試薬であるオルト酢酸エステルが活性化されます。
アルコールの脱離によって、活性試薬であるカチオン中間体が生成し、これに対して原料のアルコールが付加反応を起こして、原料を含んだオルトエステルを形成します。
さらに酸触媒によって、試薬由来の別のアルコールがこの中間体から抜け、メチル基から脱プロトン化が進行すれば、ケテンアセタールとなります。
原料を含んだこのケテンアセタールは、Claisen転位に必要なアリルビニルエーテル構造を有しており、加熱することによって6員環遷移状態を経ながら炭素-炭素結合の形成と炭素-酸素結合の切断が協奏的に進行します。
シグマトロピー転位の進行とともに単結合と二重結合の位置がひとつずつ移動し、最終的にエステルを生成物として与えます。
クライゼン転位では原料の立体化学が転写される
Claisen転位全般に言えることですが、[3,3]-シグマトロピー転位が起こる際、6員環遷移状態を経由して反応が進行します。
そのため、原料のアリルアルコールに立体中心がある場合は、Johnson-Claisen生成物に立体化学が強く反映されます。
特にオルト酢酸エステルを活性化試薬に用いた場合は生成物の立体化学を予測しやすく、不斉炭素の構築法として重要です。
アリルアルコールの炭素-炭素二重結合の幾何異性がコントロールできれば、新しくできる炭素-炭素結合の立体化学を制御できるわけです。

酢酸由来のオルトエステル以外にもより炭素鎖の長い活性化試薬も用いることができますが、こちらは中間体であるケテンアセタールの幾何異性を制御するのが難しい場合が多いです。
オルト酢酸エステル以外では、生成物がジアステレオマー混合物になりうる点は注意が必要ですね。
ジアステレオ選択的なClaisen転位は、親戚であるIreland-Claisen転位のほうが得意な印象です。
ジョンソン-クライゼン転位の進行には酸触媒が必要
一般的なJohnson-Claisen転位の注意点として、反応の進行に酸が必要であるという点が挙げられます。
最初のオルト酢酸エステルの活性化、鍵であるケテンアセタールの形成など、Claisen転位に必須のアリルビニルエーテル構造を作るためには酸が必要です。
酸に弱いなど、原料の性質によってはEschenmoser-Claisen転位やIreland-Claisen転位を使用したほうがよい例も多いでしょう。
ただ、オルトエステルは溶媒として使用するなど試薬の量を厳密にコントロールする必要もなく、酸を少量入れて加熱するだけで反応が進行しますので、操作性はIreland-Claisen転位よりも遥かに簡単でいいですね。
まとめ
Johnson-Claisen転位で得られる生成物は、程よい位置にエステルと二重結合を持っていて、いろいろな反応の中間体として利用できます。
原料のアリルアルコールも、アルデヒドに対してGrignard試薬などで簡単に、バリエーション豊かに用意でき、立体化学の転写を利用した優れた利用例がたくさん知られています。
とくにJohnson教授のグループによるステロイド合成研究では、多くの重要な炭素-炭素結合がこの反応によって作られました。
歴史的偉業を支えた反応ですね。
関連記事です。
炭素を増やしながらエステルを合成すると言えば、安定イリドを用いたWittig反応の利用が思いつきます。
こちらは炭素が減りながら転位反応が進行するCurtius転位に関する記事です。炭素-炭素結合の形成と切断はいつの時代でも合成化学者にとって重要です。
得られた生成物の二重結合を切断する際に、よくオゾン分解が用いられますね。