有機分子の中には、タンパク質などの生体内高分子に対して作用する生物活性分子が知られています。
標的タンパク質に相互作用する場合、水素結合や静電相互作用、疎水性相互作用など、特定の官能基がたんぱく質との親和性に重要な役割を果たしています。
しかし、相互作用できる官能基がただ単にそろっていれば生物活性を発揮するかと言えば全くそんなことはなく、有機分子とタンパク質、それぞれがちょうどいい「カタチ」をしていることがとても大事です。
ひものようにフラフラした鎖状化合物にも多くの生物活性分子がありますが、環状化合物は構造の自由度が制限されているため、ちょうどいい「カタチ」がより維持されやすい傾向にあります。
エリスロマイシンに代表されるマクロライド抗生物質は、大きな環状ラクトン構造を有する化合物群であり、これら一連の化合物が人類の健康に果たしてきた貢献度は計り知れないものがあります。
生合成では、これら大環状ラクトンの形成があたかも簡単かのように達成されて見えますが、合成化学者が行うには非常に大変です。
今回は、大環状ラクトンを合成したいときに最もよく使われるマクロラクトン形成法のひとつであるYamaguchi lactonization(山口ラクトン化)について考えていきましょう。
山口ラクトン化はトリクロロベンゾイルクロリドを活性化剤とするラクトン合成
山口ラクトン化では、カルボン酸の活性化剤に2,4,6-トリクロロベンゾイルクロライド(2,4,6-trichlorobenzoyl chloride)を用います。
山口ラクトン化の反応機構は二段階の分子変換で成り立っています。

まず一段階目でカルボン酸を活性化します。
原料であるセコ酸に対して、トリエチルアミンとともにベンゾイルクロライドを作用させると、トリエチルアミンにより活性化された原料のカルボン酸が、ベンゾイルクロライドに求核攻撃を起こし、混合酸無水物(mixed anhydride)中間体を与えます。
この酸無水物を二段階目の反応であるラクトン化に使用します。
N,N-ジメチル-4-アミノピリジン(DMAP)のジクロロメタンやトルエン溶液を加熱した反応溶液に対して、先ほど調製した混合酸無水物の溶液を、シリンジポンプなどでゆっくりと滴下して行きます。
すると、活性化された酸無水物に対してDMAPが作用し、カルボン酸由来のカルボニル炭素に求核攻撃を起こします。
カルボン酸にDMAPが結合した中間体は、プラスの電荷を帯びており、求電子性が非常に上がっています。
この活性種に、分子内のアルコールが求核攻撃を起こすことによって環化が進行し、DMAPのトリクロロ安息香酸塩の副生とともに、生成物であるラクトンが得られます。
3つの塩素とオルト置換基で高活性化と反応位置の制御を実現
山口法で使用される2,4,6-トリクロロベンゾイルクロライドには、ラクトン化前の活性種であるアシル化されたDMAP中間体の形成を有利にする工夫が詰まっています。
ひとつ目として、電子吸引基である塩素原子が3つも置換した安息香酸誘導体を用いることによって、トリエチルアミンで活性化されたカルボン酸誘導体(カルボキシレート)の攻撃を受けやすくしており、混合酸無水物の形成を促進しています。
続くDMAPとの反応でも、塩素の電子吸引性によって混合酸無水物は活性な状態ですので、素早くアシル置換したDMAP中間体を形成することができます。
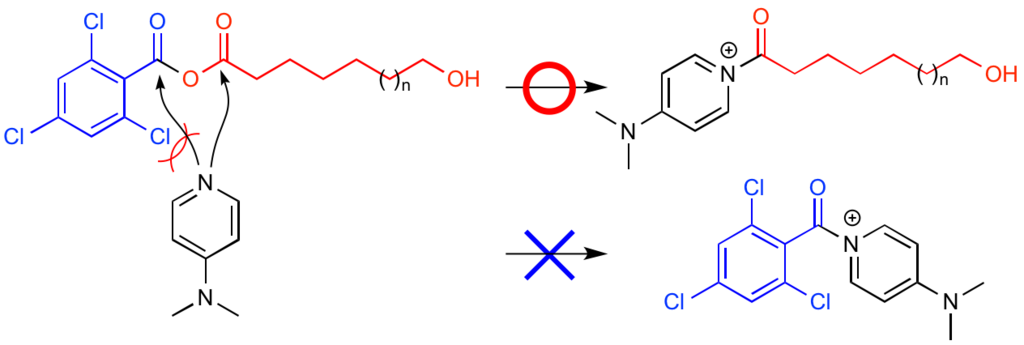
ふたつ目として、カルボン酸に対して塩素原子がオルト位に置換していることで、DMAPと反応するカルボニル基を制御しています。
酸無水物中間体にはカルボニル炭素が2つ存在していますが、立体的に大きな塩素原子の効果によって、試薬由来のカルボニル基側がブロックされており、DMAPは原料由来カルボン酸側と優先して反応します。
試薬側のカルボニル基にDMAPが求核攻撃してしまうと、分子内環化ではなくてアルコールのトリクロロベンゾイル化になってしまいますからね。
山口法を分子間反応に使えば強力なエステル合成
山口ラクトン化は文字通り、分子内でエステル結合を形成するラクトン合成が有名です。
それまでにも、様々なラクトン合成法が開発されてきましたが、山口法によるラクトン形成は一般性が高く、多くの分子の環化に成功してきました。
ですが、何も分子内反応だけでなく、カルボン酸とアルコールに対して山口法を適用すれば、分子の連結反応が進行したエステルが得られます。
反応で使用する2,4,6-トリクロロベンゾイルクロライドは反応の後処理後には安息香酸誘導体に変換されますので、反応混合物を重曹水などで抽出すれば、活性化剤由来の試薬カスは比較的容易に除去できます。
DCCとかは分離が困難な場合が多いため、エステル合成でも山口法は重宝します。
オリジナルの山口ラクトン化では、混合酸無水物を調製した後に、副生するトリエチルアミンの塩酸塩を除去する操作が、少し煩わしいのが難点ですかね。
より簡便な操作にしたYonemitsu modification(米光-山口法)も報告されていますが、そのあたりの話はまたの機会に。
まとめ
トリクロロベンゾイルクロライドを活性化剤に用いる山口マクロラクトン化は、一般性と信頼性の高いラクトン合成法として現在でもよく使われている反応のひとつです。
とらおも何度もお世話になったことがあり、非常に使いやすい反応です。
最近では椎名法が勢力を増していますが、山口法の試薬の方が少し安かった気がします。
大量合成などでは、まだまだこちらの方が使いやすいかもしれませんね。
関連記事です。
こちらはCorey-Nicolaou法によるマクロラクトン化の記事です。マクロライド合成は多くの有用反応を生み出しました。
ラクトン化の前駆体合成には、Kraus-Pinnic酸化でアルデヒドからカルボン酸を作ることも多いですね。
こちらはリン原子の酸素親和性を利用したエステル合成の代表例、光延反応のご紹介です。