有機化学において極性転換(umpolung)を用いた反応戦略は、これまでの常識をひっくり返すインパクトを提供しうるものであり、化学者のこころをワクワクさせます。
極性転換は、ある官能基の通常知られている化学的な振る舞いとは真逆の性質を与えること、とも理解でき、求電子的な官能基を求核的に、求核的な官能基を求電子的に反応させることによって、官能基が持ちうる可能性を倍に広げてくれるわけです。
生体内でも極性転換反応を利用した分子変換は利用されており、チアミン(ビタミンB1)によるピルビン酸の脱炭酸機構は有名ですね。
また、芳香族アルデヒドはカルボニルのα位に水素原子を持たず、加えて芳香環とアルデヒドが共鳴構造を取りうるため、特異な反応を可能にする場合があります。
Cannizzaro反応では水酸化物イオンの付加により分子が活性化され、芳香族アルデヒド由来の水素原子がヒドリドとしてもう一分子のアルデヒドを還元しています。
本日は、極性転換を利用した芳香族アルデヒドの二量化反応のひとつであるbenzoin condensation(ベンゾイン縮合)について考えていきたいと思います。
ベンゾイン縮合では片方のアルデヒドが極性転換により求核剤になる
ベンズアルデヒドなどの芳香族アルデヒドに対して、含水エタノール中でシアン化カリウム(KCN)やシアン化ナトリウム(NaCN)を作用させると、2分子の原料が縮合反応を起こし、二量体であるベンゾインを与えます。

このベンゾイン縮合の反応機構は次のように考えられています。
まず、求核性に優れたシアン化物イオンがアルデヒドに対して付加反応を起こし、シアノヒドリンを形成します。
脂肪族アルデヒドの場合では、対応するシアノヒドリンを生成物として回収することが多いのですが、芳香族シアノヒドリンではさらに反応を進行させることができます。
芳香族シアノヒドリンの水素原子は、芳香環のα位であるためプロトンとして引き抜かれやすい性質が元々あるのですが、付加したシアノ基の電子吸引性により、さらに強力に酸性度が上がっています。
そのため、系内の塩基によって脱プロトン化が進行すれば、カルボアニオンを発生することができます。
このカルボアニオンがもう一分子の芳香族アルデヒドに対して付加反応を起こすと、炭素-炭素結合が形成されたアルコキシドを与えます。
アルコキシドがシアノヒドリンの水酸基からプロトンを奪った場合、脱離基としても優れているシアノ基を分子外に押し出すように反応が進行して、ベンゾインを形成するわけです。
ベンゾイン縮合の反応の前後をみると、シアン化物イオンは触媒として働き、2分子のアルデヒドのうち片方がアシルアニオンとして、もう一つが本来の求電子的なアルデヒドとして連結反応を起こしたことがわかります。
反応のポイントは、シアノ基によるカルボアニオンの安定化です。
この効果により、もともとカルボニル炭素だった位置が求核剤として反応できるようになっていますね。
チアミンやNHC触媒でもベンゾイン縮合は進行する
ピルビン酸の脱炭酸で重要な働きを示したチアミンもベンゾイン縮合に使用することができます。
チアミンなどのチアゾリウム塩を塩基性条件で処理すると、硫黄と窒素原子に挟まれた炭素上に二配位炭素であるカルベンが発生します。
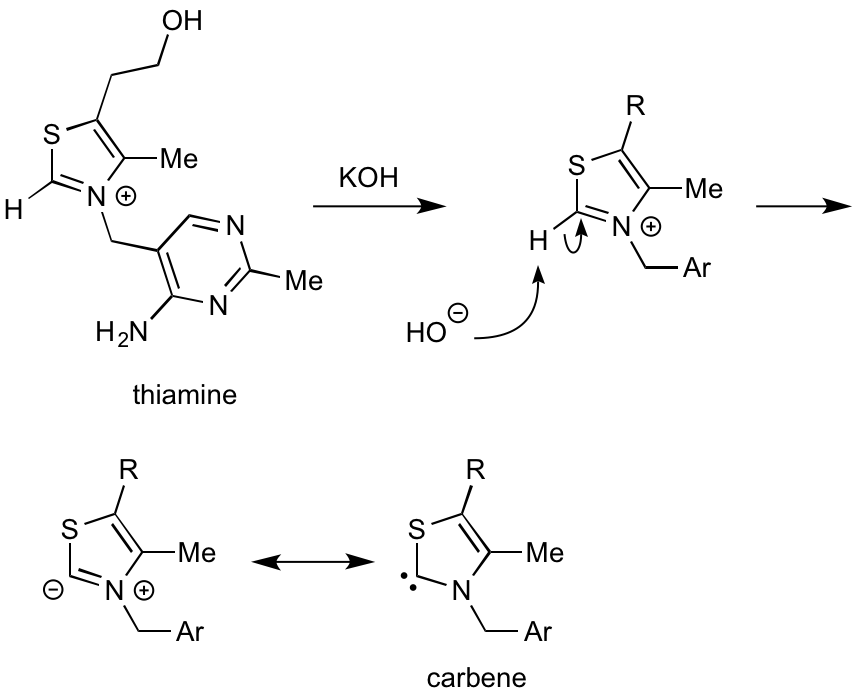
カルベンは電気的に中性の化学種ですが、価電子が6個しかない点ではカルボカチオンと同様で、また共有結合も2つしかないため非共有電子対を有しているためカルボアニオンとも共通点があります。
つまりカルベンは、カチオンとアニオン、両方の性質を兼ね備えた化学種になるわけですが、このカルベンがベンゾイン縮合を進行させます。

芳香族アルデヒドに対して、チアゾリウム塩から発生させたカルベンが付加反応を起こすと、アルデヒドはマイナス電荷を帯びたアルコキシドになるわけですが、カルベンはバランスをとっていたアニオンの電荷を失いますので、カルベン炭素はプラス電荷のカルボカチオンとして振舞います。
原料側の炭素にはアルデヒド由来の水素原子があるわけですが、隣の炭素がカルボカチオンですので、この水素原子はプロトンとして奪われやすく、アルコキシドが攻撃することにより、中性の中間体になります。
この中間体は、窒素原子から見れば、エナミン構造をしており、窒素原子からの電子の押し込みにより、もう一分子のアルデヒドに付加反応を起こして、炭素-炭素結合を形成します。
シアン化物イオンのベンゾイン縮合と同様に、アルコキシドが隣の水酸基からプロトンを奪うとすると、イミニウムカチオンになったチアゾリウム部分を脱離させるようにカルボニル基が形成され、チアゾリウムカルベンの再生とともに生成物であるベンゾインを与えます。
近年では、より試薬の調製がしやすいN-ヘテロ環状カルベン(N-heterocyclic carbene: NHC)が同様の目的で活用され、関連する反応の不斉触媒として多く利用されていますね。
まとめ
ベンゾイン縮合はシアン化物イオンによる極性転換を受けたアルデヒドがもう1分子のアルデヒドと二量化する反応です。
関連するStetter反応ではα,β-不飽和カルボニルへの付加反応を実現していますね。
アルデヒドへの求核攻撃、カルボアニオンを安定化する仕組み、炭素-炭素結合形成後に脱離できる能力、これらが備わっているチアゾリウム塩やイミダゾリウム塩から発生されるカルベンは、毒性の高いシアン化物イオンの代わりとして最適です。
不斉触媒への応用も広く展開されていますが、カルベンに潜在する可能性はまだまだ広がりそうです。
関連記事です。
芳香族アルデヒドでよく見られるCannizzaroに関する記事です。アルデヒド由来の水素原子がヒドリドとして利用されていますね。
こちらもアルデヒド分子の二量化反応のひとつであるTishchenko反応の紹介記事です。
Evans-Tishchenko反応ではβ-ヒドロキシケトンを利用した立体選択的還元反応が進行し、1,3-ジオールが得られます。