炭素-炭素二重結合であるオレフィンには、電子豊富なもの、普通のもの、電子不足のものといった電子的性質が異なるオレフィンがあります。
例えば、α,β-不飽和ケトンなど電子吸引性官能基が直結したオレフィンでは、隣接基の影響で二重結合を形成しているπ電子の雲が薄くなっている状態です。
これらのオレフィンに対しては、電子を与えたがっている求核的な反応試薬が電子雲の薄い箇所を狙って飛び込んでくるわけです。
一方で、シリルエノールエーテルに含まれる炭素-炭素二重結合などは、非共有電子対を2つもつ酸素原子からの電子の押し込みにより電子の雲が分厚くなっていて、電子を欲しがっている求電子剤と素早く反応することが知られています。
今回は、シリルエノールエーテルからα-シリルオキシケトンを合成できるRubottom oxidation(ルボトム酸化)について考えたいと思います。
電子豊富なシリルエノールエーテルのエポキシ化を経由するルボトム酸化
ケトンのα位(隣の炭素)は、電子吸引性カルボニル基の影響によって、水素の酸性度が高く、プロトンとして奪われやすい状態になっています。

そのため、LDAやLiHMDSなどのかさ高い強塩基を作用させると、ケトンのα位炭素から脱プロトン化が進行したリチウムエノラートが比較的簡単に形成できます。
このエノラートに対してトリメチルクロロシラン(TMSCl)などのシリル化剤を作用させると、酸素親和性の高いケイ素原子がアニオン化した酸素を捕捉して、シリルエノールエーテルが得られるわけです。

ここからがようやくRubottom酸化なわけですが、得られたシリルエノールエーテルに対してメタクロロ過安息香酸(m-CPBA)を作用させると、m-CPBAに含まれる弱い酸素-酸素結合を切断するように、電子豊富なオレフィンから電子が供給され、エポキシド(シリルオキシオキシラン)を形成できます。
ただ、カルボン酸の一種でもあるm-CPBAを使った場合、m-CPBAあるいは酸素を供給し終わったm-CBA(メタクロロ安息香酸)の酸性によって、不安定なエポキシド中間体構造は分解してしまうんです。
エポキシドの両端炭素原子のうち、シリルオキシ基がついた方はアセタール構造になっているため、酸素原子からの電子の押し込みが強く、結果として、シリル基で安定化されたオキソニウムカチオンとアルコールを与えます。
1,4位の関係にある酸素原子間でシリル基が移動したとすると、不安定なカチオン中間体を解消できるため、中性分子を目指したシリル基転位によって生成物であるα-シリルオキシケトンが得られます。
最終的には転位したシリル基も除去して、α-ヒドロキシケトンとして単離することも多い反応ですね。
エポキシ化の面選択性がα-ヒドロキシケトンの立体化学を決定する
シリルエノールエーテルとしてよく使われるのは、TMSやトリエチルシリル(TES)基が置換したものが多い印象ですね。
エポキシ化、シリル基転位の2つの段階が立体障害と電子的な要因で遅くなるため、TES基より大きいTBS、TIPS、TBDPS基などが使われることは稀だと思います。
Rubottom酸化の大事な特徴として、エポキシドの立体化学がそのまま最終生成物のアルコールに引き継がれる点が挙げられます。
反応機構からも推察できますが、最終生成物のケトンのα位に相当する炭素上の立体化学はエポキシ化の段階から変わっていません。
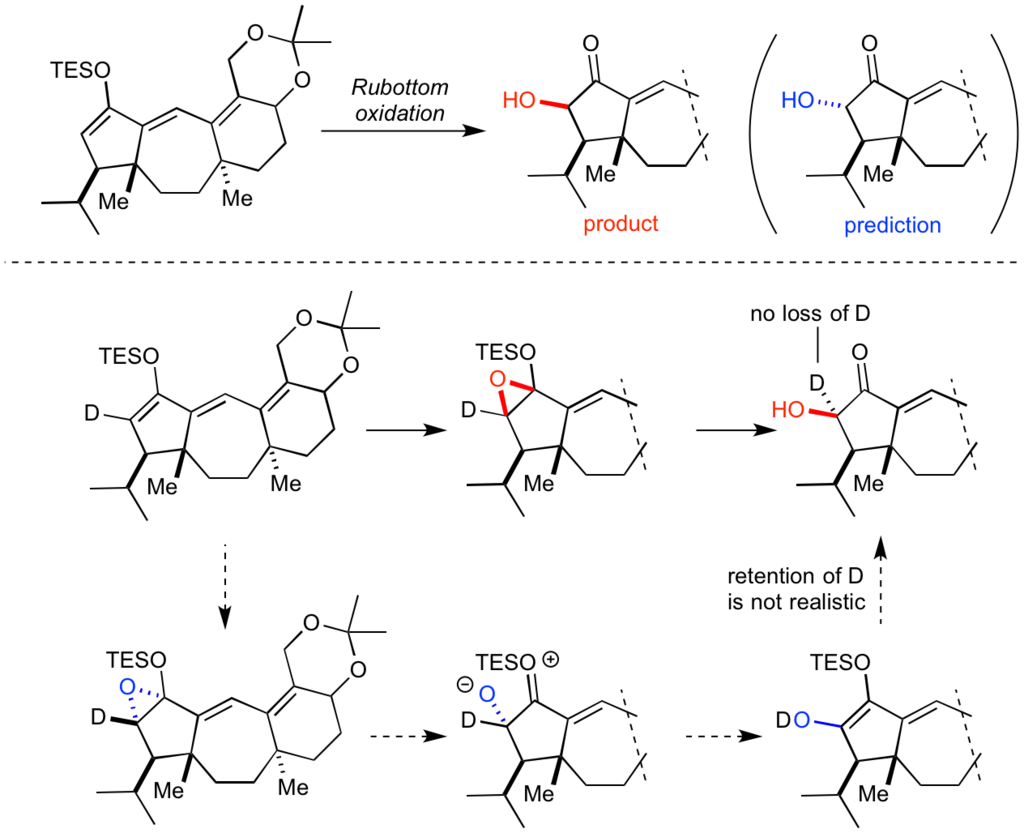
例えば、Guanacastepeneの合成研究において、Danishafsky先生らは予想とは異なるRubottom酸化生成物を得ました。
彼らは当初、Rubottom酸化進行後にケトンのα位が異性化したようにも考えたようです。
しかし、重水素(D)を用いた実験によって、エポキシ化が予想外の面から進行しただけでRubottom酸化はきちんとエポキシドの立体化学をそのまま生成物に引き継いでいることが確認されました。
S. J. Danishefsky, et. al. Tetrahedron Lett., 2004, 24, 3831-3833
なので、望みの立体化学を有する最終生成物を得るには、エポキシ化をきちんと制御する必要があるということですね。
中性のDMDOを使えば不安定中間体も単離可能
Rubottom酸化の多くの場合、m-CPBAを酸化剤として用いますが、上にあるように試薬の酸性によって、シリル基の転位反応が促進されてしまいます。
一方で、ジメチルジオキシラン(DMDO)をm-CPBAの代わりに使うことによって、中間体エポキシドであるシリルオキシオキシランが得られる場合があります。
中性の酸化剤であるDMDOは、他の酸化剤では成し得ない分子変換を実現してくれることがあります。
ただし作るのが大変で、酸化力も強いため取り扱いに注意が必要ですね。
Rubottom酸化ではだいたいm-CPBAかDMDOを使えば、間違いないでしょう。
まとめ
シリルエノールエーテルは、ケトンからだけでなくエノンの1,4-還元と続くシリル化などでも得られる有用中間体で、位置選択的な合成法が色々と開発されています。
汎用性の高い中間体と組み合わせることで、Rubottom酸化の信頼性も合わせて向上していますね。
原料の他の部分にもオレフィンがある場合は、酸化力の強いm-CPBAやDMDOを使ったRubottom酸化が向いていない場合があります。
そんなときはDavis酸化反応を使うなど、原料の性質に合わせて反応条件を相補的に使って行きたいものです。
関連記事です。
m-CPBAを使った有用反応の一つにBaeyer-Villiger酸化がありますね。ラクトンや3級アルコールの立体選択的な合成に有用です。
より強いオゾン酸化では二重結合の切断や炭素-水素結合の直接酸化も達成できます。
色々な酸化反応を実現できる超原子価ヨウ素試薬であるIBXに関する記事です。