有機合成において、多くの官能基が存在する中で狙った部分だけを反応させることができる試薬・反応は、大変重宝されます。
例えばアルコールをアルデヒドやケトンに変換する酸化剤は、化学史上多数存在します。
しかし、現在でも使用されている試薬のほとんどは、アルコール以外とは反応しないという官能基選択性に優れたものに淘汰されています。
今回は、アルデヒドをカルボン酸に酸化する方法の中でも、官能基選択性が高い数少ない定法のひとつであるKraus-Pinnick酸化(クラウス-ピニック酸化)について考えていきたいと思います。
亜塩素酸が可能にするアルデヒドからカルボン酸への選択的酸化
亜塩素酸ナトリウムを利用したアルデヒドからカルボン酸への酸化反応は、Lindgrenらによってバニリンのバニリン酸への変換に利用されたのが、最初の報告であるとされています。
その後、後述するように現在でも広く使われている、2-メチル-2-ブテンを塩素のスカベンジャーに使う条件がKrausグループによって発表され、副反応を起こし易かった二重結合を有する原料へも適応範囲が広がりました。
ただ、現在ではPinnick酸化とよく呼ばれるように、のちにPinnickらによって本反応の有用性が広く知れ渡るところとなり、アルデヒドからカルボン酸への反応の定法として定着していったようです。
本来は、Lindgren-Kraus酸化、あるいはLindgren-Kraus-Pinnick酸化とすべきかも知れませんが、本ブログではKraus-Pinnick酸化と呼ぶことにします。
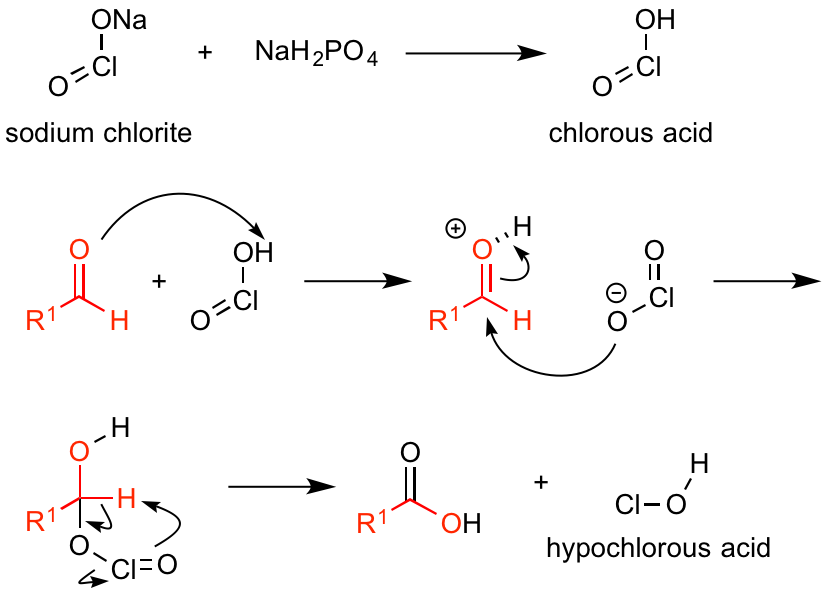
本反応はまず、弱酸性リン酸塩であるリン酸二水素ナトリウムと亜塩素酸ナトリウムの混合により、活性種である亜塩素酸を発生させます。
生じた亜塩素酸が原料であるアルデヒドに作用すると、酸によるカルボニル基の活性化の後、亜塩素酸イオンがアルデヒドに付加反応を起こして、ヘミアセタール中間体へ移行します。
このヘミアセタールから酸化が起こるわけですが、ヘミアセタール炭素からの水素原子の引き抜き、C=O 二重結合形成、O-Cl 結合の開裂が協奏的に進行するとされています。
このペリ環状反応機構によって、次亜塩素酸の放出とともに、生成物のカルボン酸が得られます。
次亜塩素酸の補足でカルボン酸合成の適用範囲が拡大

Krausが報告した2-メチル-2-ブテン添加の素晴らしいのは、副生成物である次亜塩素酸を効果的に補足するスカベンジャーとして機能する点です。
本反応では、使用直前に混合させたリン酸二水素ナトリウムと亜塩素酸ナトリウムの水溶液を、アルデヒドのt-BuOH溶液に滴下していく実験操作が推奨されています。
しかし、反応系内に次亜塩素酸が残っていると、新たに滴下された亜塩素酸が次亜塩素酸によって分解されてしまい、酸化能力のない二酸化塩素(chlorine dioxide)に変化してしまいます。
また、次亜塩素酸は炭素-炭素二重結合であるオレフィンとも反応でき、クロロヒドリンを与える副反応も進行してしまいます。そのため、酸化させたいアルデヒドにオレフィンがある場合、クロロヒドリン形成が問題となるわけです。
三置換オレフィンである2-メチル-2-ブテンがスカベンジャーとして過剰量反応系内に存在すると、諸悪の根源である次亜塩素酸を効率的に補足し、対応するクロロヒドリンへ変換してくれます。
おかげで、次亜塩素酸が反応系から除去され、余計な副反応が起こらずに済むんですね。ありがたい。
まとめ
1級アルコールから直接カルボン酸まで酸化できる方法が、近年活発に研究され実用化されてきました。
しかしながら、オレフィンのオゾン分解など他の官能基からアルデヒドを経由し、カルボン酸へ誘導したいという要請は根強く、官能基選択的なアルデヒドの酸化反応はこれからも重宝されると思います。
アルデヒドからカルボン酸に変換できる方法として、酸化銀(I)を使う方法やDMF中でOxone ®を作用させる方法がありますが、簡便さや試薬の値段など、今のところ私の中ではKraus-Pinnick酸化の一択ですね。
逆に考えれば、これを上回る簡単さと安さ、官能基選択性を実現できれば、一気に市場を独占できる可能性があり、挑戦し甲斐のある変換反応のひとつと言えますね。
関連記事です。
アルコールをアルデヒドに酸化する定番反応のDess-Martin試薬の紹介記事です。室温でパッと混ぜるだけなので、とらおみたいなズボラ化学者の親友ですな。
Jones酸化は1級アルコールから一段階でカルボン酸まで酸化できる便利な酸化剤ですね。酸性条件に耐えられる場合はこちらを利用も候補になります。
クロム酸を使う酸化剤ではCorey先生が開発されたPDCが、とらお的には好きです。
www.tora-organic.com