硫黄は周期表の第3周期の元素であり、炭素や酸素、窒素原子など第2周期とは異なる化学的性質を示します。
同じ第16族元素である酸素とよく比較されますが、とらおの理解を大雑把に言えば、価電子の数は一緒だが、化学反応に関わる軌道の大きさ(酸素:2s, 2p軌道;硫黄:3s, 3p軌道)が異なる、ということです。
特に軌道の大きさが異なる性質は、ブレンステッド酸やルイス酸に対する親和性、隣の化学種(カチオンやアニオン、ラジカル等)への相互作用の仕方に違いを生み出し、有機合成の多様性、可能性を広げてくれています。
本日は、そんな硫黄原子が二つも入ったジチアンを使った有機化学について考えてみたいと思います。
Corey-Seebach反応はジチアンを利用したアルデヒドの極性転換反応

6員環に2つの硫黄原子が含まれるジチアンの中でも、1,3-ジチアンはカルボニル基の保護基として使われるケタール誘導体です。
2つの硫黄原子で挟まれた炭素原子の性質がおもしろいわけですが、1,3-ジチアンの化学は、E. J. Corey先生とDieter Seebach先生(ディーター・ゼーバッハ先生)らの研究によって大きく花開き、現在でも有用な分子変換として使われています。
カルボニル基はC=O二重結合を有する官能基であり、電気陰性度のバランスから酸素がマイナス、炭素原子がプラスに分極した特徴を持っています。
そのため、マイナス性を帯びた求核剤はカルボニルの炭素原子に求核攻撃を起こしやすく、様々な化学反応に利用されています。
一方でCorey先生らは、アルデヒドから誘導できる1,3-ジチアンの2位の炭素は、強塩基であるブチルリチウムを作用させると脱プロトン化が進行し、生じたカルボアニオンが様々な求電子剤と反応することを見出しました。

アルデヒドから誘導できる1,3-ジチアンの2位の炭素は、二つの硫黄原子に挟まれている影響で、pKaが約31とかなり酸性度の高い水素原子を有していることになります。
仮に1,3-ジチアンの2位にアニオンが発生したとすると、その隣の炭素-硫黄の反結合性軌道であるσ*軌道がカルボアニオンを安定化するため、2位のプロトンの酸性度が上がっているわけです。
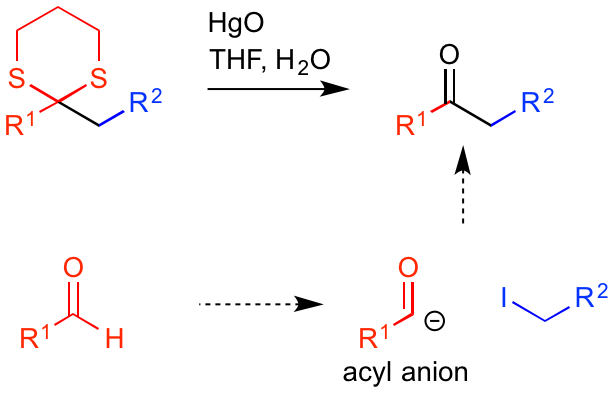
反応後にジチアンを除去すればケトンが得られるため、形式的にはアルデヒドの水素原子が脱プロトン化されたアシルアニオンとして反応したと考えることができます。
そのため、求電子的なアルデヒドが求核的なアシルアニオンに変わったことになりますね。
その後、Seebach先生はこの反応を起点として、より一般的な極性転換(Umpolung)として体系化し、多くの化学者に注目されるコンセプトとして今日でも発展し続けていますね。
1,3-ジチアンの優秀なところは、大きな分子の部分構造の連結に使えることに加えて、生成物でのジチアンの特殊な化学反応性から、すぐに脱保護してケトンにしてもいいし、そのまま残していても多くの反応に耐えられる、というところだと思います。
脱保護に苦労する1,3-ジチアン
ジチアンを使ったカップリング反応では、ブチルリチウムに代表される強塩基を使うため、適切な反応条件を必要とするのはもちろんなのですが、以外に大変なのがジチアンの除去です。
軌道相互作用の違いから、硫黄原子はプロトンやよく用いられるルイス酸ではあまり活性化されません。

例えばアルデヒドからジチアンを作る際には、1,3-プロパンジチオールをトシル酸(TsOH)やBF3·OEt2とともに処理すれば、割と簡単に形成できます。
これは、脱離させたい酸素原子の活性化にプロトンやBF3·OEt2などが適しているため、カルボニルの求電子性が上がり、チオールの付加反応を促進しています。
一方で、ジチアンの脱保護には硫黄原子を活性化する必要があるのですが、最も効果的なのは水銀イオンを用いる活性化です。
ソフトなルイス塩基である硫黄原子の活性化には、ソフトなルイス酸が必要となるわけです。
ただ、水銀は毒性と処理の関係でなかなか使いづらい試薬であるため、多くの化学者が尻込みしてしまいます。

代わりによく用いられる脱保護の条件は、ヨードメタンを活性化剤として含水アセトンやアセトニトリル中で炭酸カルシウムなどの塩基とともに処理するものです。
硫黄原子は酸素などと比較してアルキル化されやすく、特にヨードメタンによって片方のスルフィドがメチル化されれば、他方のスルフィドからの電子の押し込みにより、カルボカチオンを発生できます。
水分子がカルボカチオンに付加すれば、ヘミチオケタールになり酸素原子がチオールを押し出すようにプロパンジチオールが外れ、ケトンを得られるわけです。
ただし、ヨードメタンも発がん性が気になる試薬ですので、値段が高いですがPIFA([bis(trifluoroacetoxy)iodo]benzene)など、より安全な試薬を先に試すほうがいいかもしれません。
個人的には、試薬としても安いヨウ素分子を活性化剤に使うことが多いですかね。
1,3-ジチアンを使った最近の例で、A. B. Smith先生らによるブルック転位(Brook rearrangement)をうまく使ったアニオンリレー化学も発展していますが、そのあたりの話は、またの機会に。
まとめ
今日でもよく活用されているコンセプトである極性転換(Umpolung)。その発展の発端となった1,3-ジチアンの化学は、硫黄の特性を利用した化学といえますね。
似たような働きができそうな5員環バージョン1,3-ジチオランは、アニオンの安定性が悪くエチレンガスとジチオカルボキシラートに分解してしまうようです。
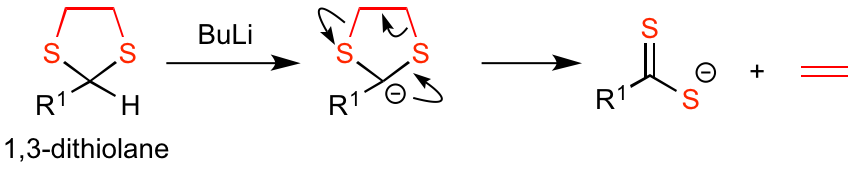
炭素-硫黄結合のσ*軌道がカルボアニオンの安定化にも寄与していますので、6員環に深い意味があるんですねー。
関連記事です。
ジチアンと並んでカルボニルの極性転換に使われるシアノヒドリンに関する記事です。こちらも分子のカップリングによく使われますね。
ベンゾイン縮合では反応系内で極性転換と脱保護がスマートに進行していますね。
スルフィドの有用な使い道としてPummerer転位は外せません。