カルボニル化合物は、数ある置換基の中でも最も基本的な官能基のひとつであり、様々な化学反応に利用されています。
もし、二つのカルボニル化合物を同じフラスコ内で、区別しながら連結することができれば、多数の有用な官能基を有する生成物が一挙に得られ、合成効率と応用性が格段に広がります。
今日は、α,β-不飽和カルボニル化合物とアルデヒドを炭素-炭素結合の形成をしながら連結できるMorita-Baylis-Hillman反応(森田-ベイリス-ヒルマン反応)について、考えていきましょう。
3級アミンが活躍する炭素-炭素連結反応

Morita-Baylis-Hillman反応は、α,β-不飽和エステル(acrylate)などの活性化された二重結合とアルデヒドが3級アミンもしくは3級ホスフィン触媒の作用によって連結する反応です。
本反応で主に使われる触媒は、DABCOと呼ばれる環状三級アミンです。
このDABCO(1,4-ジアザビシクロ[2.2.2]オクタン)はピペラジンがもう一つメチレン鎖で架橋されたアミンで、窒素原子周りの炭素鎖が後ろ手に縛られた状態であり、立体障害が小さく求核性に優れた特徴を有します。
このアミンがまず、α,β-不飽和エステルに対して1,4-付加(Michael付加)を起こし、窒素上にプラス電荷、エステル由来のエノラートにマイナス電荷が乗った、双性イオン(ベタイン)になります。
中間体のエノラート部分が、カップリング相手であるアルデヒドに対してアルドール(aldol)反応を起こして、β-アルコキシエステルを生じます。
次いで、最終生成物にあるα,β-不飽和エステル構造を再構築するため、プロトン移動とDABCOの脱離が進行し、2つのカルボニル化合物の連結とDABCOが触媒として再び働きに行けるようになります。
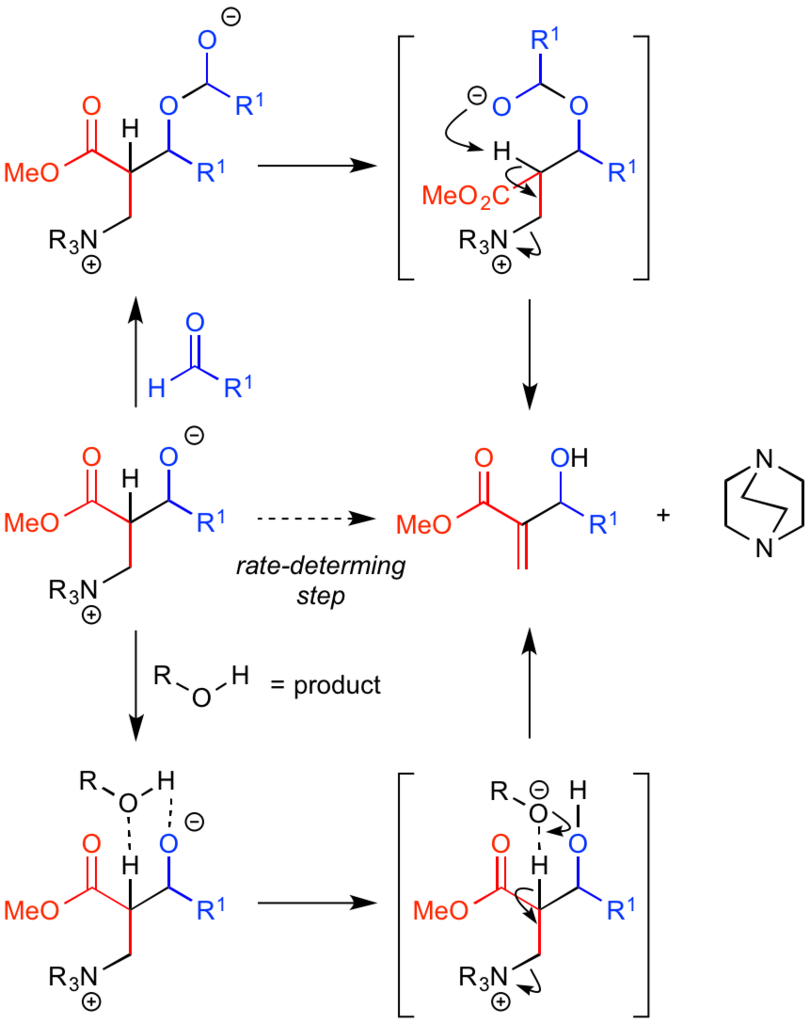
反応機構はまだハッキリ分かっていないようですが、反応全体の律速段階はアルドール付加体からDABCOの脱離段階に必要な、プロトン移動過程だと推測されています。
McQuadeとAggarwalらによれば、Morita-Baylis-Hillman反応は求電子剤であるアルデヒドに対して2次、DABCOとアクリレートに対して1次の反応であり、アルドール付加体のアルコキシドに対して、もう1分子のアルデヒドが作用し、ヘミアセタールのアニオンが6員環遷移状態を取りながらエステルのα位からプロトンを引き抜き、生成物へと移行していると提唱しています。
さらに、Morita-Baylis-Hillman反応は反応が進行するに従って加速する自己触媒効果が観測されるようですが、Aggarwalらによれば、生成物に含まれるアルコール部分が律速段階のプロトン移動を加速する別の経路が派生し、二つの反応経路で生成物を与えていると考えられます。
ただ、これらのメカニズムでも説明できないことがあるようで、議論は終結していません。
添加剤のちからで超低速反応をスピードアップ
α,β-不飽和エステル以外にも、エステル部分がアミド、ニトリル、スルホン、ホスフェート、ニトロ、アルデヒド、ケトンなど、多様な電子吸引基で活性化されたα,β-不飽和化合物に対して本反応の応用が可能です。
求電子剤としては主にアルデヒドが用いられますが、加圧条件など場合によってはケトンへの求核攻撃を起こさせることもでき、アリル基の導入やアルキル化の例も報告されています。

求電子剤の重要な応用例として、イミンを求電子剤として用いるaza-Morita-Baylis-Hillman反応が挙げられます。
特に窒素上に電子吸引基が置換されたイミンは活性であり、生成物としてアリルアミン誘導体を与える有用な反応です。
Morita-Baylis-Hillman反応の最大の弱点は、反応速度が遅いことです。
反応の全行程が平衡反応であり、生成物からも逆反応により原料へ戻りうるようですが、平衡状態に達するまで相当な時間がかかる場合が多いです。
反応速度を上げるため、様々な工夫がなされてきましたが、中でもルイス酸やブレンステッド酸などの添加剤が有効に作用することが知られています。
ただし、強すぎる酸は、DABCOに代表される3級アミンやホスフィン触媒の触媒毒になるため、本反応には使えません。
また、溶媒による反応速度の違いも顕著です。
反応機構のところでも少し触れましたが、アルコールや水の存在が律速段階の促進に有効であり、特にジオキサン:水=1:1の溶媒系ではDABCOが1当量必要ではあるものの、反応が大幅に加速されるようです。
今のところ、原料である活性α,β-不飽和化合物と求電子剤の組み合わせによって、最適な反応条件を精査する必要があり、万能触媒・万能条件の開発が強く望まれますね。
まとめ
Morita-Baylis-Hillman反応は、ほぼ中性条件で2つの有用なビルディングプロックを連結でき、かつ高い応用性を秘めた官能基を携えた生成物を与える優れた反応です。
本反応は3級アミンを使う条件が一般的ですが、個人的に伊藤グループによって報告されたジメチルフェニルホスフィンを用いる条件に、何度も助けられました。
試薬が酸化されやすいですが、オススメですね。
関連記事です。
Mannich反応もカルボニル化合物からの分子変換として大切ですね。
こちらはEshenmoser反応に関する記事です。やっぱりカルボニルを使った有機合成は幅広いですね。
Robinson環化は6員環エノンを得るための重要な連続反応です。Morita-Baylis-Hillman反応とは不飽和カルボニル化合物の役割が逆転している点も面白いですね。